

 |
 |
Метод молекулярных орбиталей исходит из того, что каждую молекулярную орбиталь представляют в виде алгебраической суммы (линейной комбинации) атомных орбиталей. Например, в молекуле водорода в образовании МО могут участвовать только
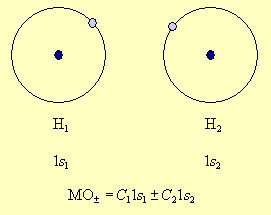 |
| Рисунок 3.6 |
Поскольку ядра во взаимодействующих атомах водорода одинаковы, то и вклад атомных орбиталей будет одинаковым, что обеспечивается равенством коэффициентов, с которыми 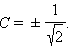 Опуская этот нормировочный множитель, запишем две молекулярные орбитали как сумму и разность АО атомов водорода:
Опуская этот нормировочный множитель, запишем две молекулярные орбитали как сумму и разность АО атомов водорода:
|
Электронная плотность этих двух состояний пропорциональна |MO±|2. Поскольку в молекуле водорода взаимодействие возможно только по оси молекулы, то каждая из MO± может быть переобозначена как σсв =
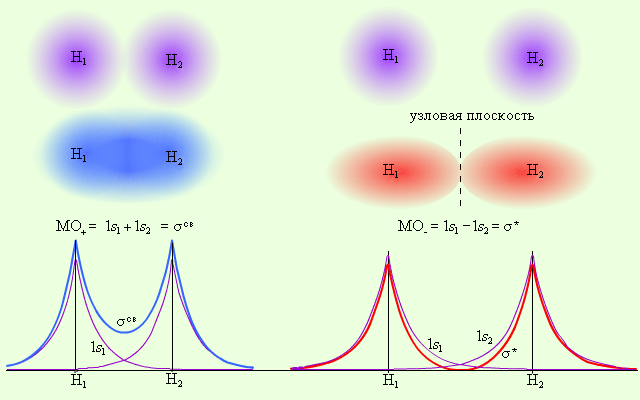 |
| Рисунок 3.7 Распределение электронной плотности в молекуле H2 |
Из рис. 3.7 видно, что электронная плотность посередине между ядрами для σсв значительна, а для σ* равна нулю. Отрицательно заряженное электронное облако, сконцентрированное в межъядерном пространстве, притягивает положительно заряженные ядра и соответствует связывающей молекулярной орбитали σсв. А МО с нулевой плотностью в межъядерном пространстве соответствует разрыхляющей орбитали σ*. Состояния σсв и σ* отвечают разным уровням энергии, причем молекулярная орбиталь σсв имеет более низкую энергию по сравнению с исходными АО двух невзаимодействующих атомов водорода
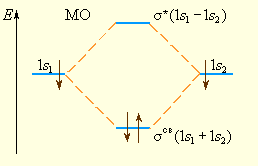 |
| Рисунок 3.8 Энергетическая диаграмма атомных и молекулярных уровней водорода
|
Переход двух электронов на МО σсв способствует понижению энергии системы; этот энергетический выигрыш равен энергии связи между атомами в молекуле водорода H–H. Даже удаление одного электрона с МО (σсв)2 c образованием (σсв)1 в молекулярном ионе
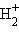 оставляет эту систему более устойчивой, чем отдельно существующие атом H и ион H+.
оставляет эту систему более устойчивой, чем отдельно существующие атом H и ион H+.
Рис. 3.9 иллюстрирует изменение энергии МО σсв и σ* в зависимости от межатомного расстояния 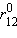 энергия σсв достигнет минимума и будет соответствовать энергии связи
энергия σсв достигнет минимума и будет соответствовать энергии связи 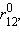 соответствующего минимуму энергии
соответствующего минимуму энергии 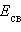 .
.
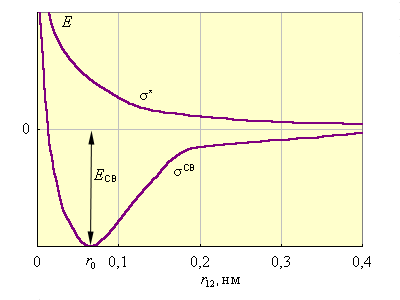 |
| Рисунок 3.9 Энергии МО в H2 в зависимости от межъядерного расстояния.
|
Приведенная на рис. 3.9 энергетическая диаграмма МО справедлива для двухъядерных образований 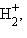
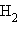 , HHe,
, HHe, 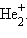 Распределение валентных электронов по МО записывают электронными формулами:
Распределение валентных электронов по МО записывают электронными формулами:
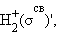
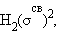
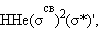
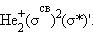
Заселение электронами связывающей МО σсв стабилизирует систему, а заселение разрыхляющих – дестабилизирует ее (табл. 3.1).
|
|||||||||||||||||||||||||||||||||||
| Таблица 3.1 Энергия, длина и порядок связи в молекулах элементов 1 периода
|
|||||||||||||||||||||||||||||||||||
Согласно методу МО порядок (кратность) связи
|
При нулевой кратности связи, как в случае He2, молекула не образуется.

 |
|
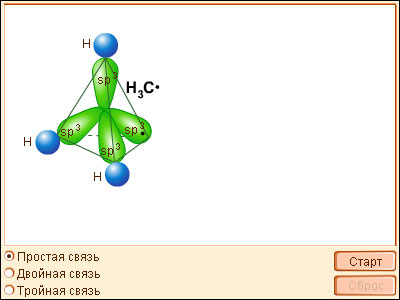
Модель 3.3.
Сигма- и пи-связи
|
 |
 |
 |

