

 Задачи с решениями
Задачи с решениями

Вычислите изменение стандартной энергии Гиббса и определите возможность протекания реакции при стандартных условиях:
| Fe2O3(т) + 3H2(г) = 2Fe(т) + 3H2O(г). |
| Fe2O3(т) | H2(г) | Fe(т) | H2O(г) | |
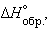 кДж∙моль–1 кДж∙моль–1 |
–822,7 | 0 | 0 | –242 |
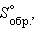 кДж∙моль–1∙K–1 кДж∙моль–1∙K–1 |
87,5 | 130,7 | 27,2 | 189 |
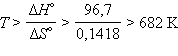 реакция становится возможной.
реакция становится возможной. 5 из 10
5 из 10
 |