

 |
 |
Химические свойства комплексного иона с известной электронной конфигурацией и геометрическим строением определяются двумя факторами: а) способностью равновесной системы при определенных условиях к превращениям; б) скоростью, с которой могут происходить превращения, ведущие к достижению равновесного состояния системы.
Первый определяет термодинамическую, а второй – кинетическую устойчивость комплексного соединения. Кинетическая устойчивость зависит от многих факторов, поэтому обычно поддается лишь качественной оценке.
В противоположность ей термодинамическая устойчивость может быть легко охарактеризована количественно с помощью констант равновесия.
В растворе ион металла M и монодентатный лиганд L взаимодействуют ступенчато с образованием комплексного иона [ML
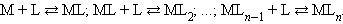 |
 |
Поскольку в этой системе существует лишь 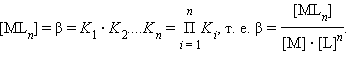
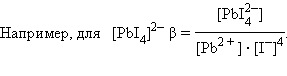
Чем больше константа устойчивости, тем более прочным является данный комплекс, поскольку
Образование прочных комплексных ионов может быть использовано для растворения труднорастворимых электролитов. Концентрация ионов в растворе определяется величиной произведения растворимости такого электролита. Добавляя в раствор вещества, образующие с одним из его ионов комплексное соединение, можно во многих случаях достичь растворения осадка за счет комплексообразования. Добиться этого тем легче, чем больше величина произведения растворимости и чем больше константа устойчивости комплексного иона. Например, хлорид серебра AgCl растворяется в избытке аммиака, образуя
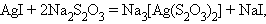 |
Комплексные ионы участвуют в реакциях обмена с образованием более прочного или менее растворимого соединения:
|
Здесь M = Ni2+, Cu2+, Fe2+.
 |
 |
 |

