Глава 9. Координационные соединения
9.7. Координационные соединения p- и s-элементов
Координационные соединения p-элементов отличаются одной особенностью по сравнению с комплексами d-металлов: комплексообразователь не содержит неспаренных электронов, поэтому к ним не применима теория кристаллического поля. Они менее многочисленны, чем комплексы d-элементов, но их представители играют весьма существенную роль в промышленных реакциях и процессах жизнедеятельности.
Как уже указывалось в начале главы, наиболее известным примером комплексного катиона служит ион аммония 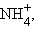 в котором реализуется
в котором реализуется 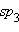 -гибридизация. Комплексный анион
-гибридизация. Комплексный анион 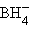 с той же
с той же 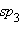 -гибридизацией образует солеобразные соединения
-гибридизацией образует солеобразные соединения 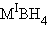 .
.
Октаэдрические комплексы с σ-связями образуют p-элементы, начиная с третьего периода: [AlF]3–, [SiF6]2–, [PF6]–; K3[AlF6] используется при электрохимическом получении алюминия, а соединения, в которые входит комплексный анион [SnCl6]2–, используются в некоторых каталитических процессах.
Из координационных соединений s-элементов следует упомянуть хлорофилл – Mg-порфириновые соединения (основной компонент фотосинтеза) и валиномицины – полиэфиры производные одноосновных карбоновых кислот (ионофоры) – способные к селективному связыванию K+.






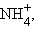 в котором реализуется
в котором реализуется 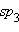 -гибридизация. Комплексный анион
-гибридизация. Комплексный анион 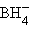 с той же
с той же 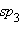 -гибридизацией образует солеобразные соединения
-гибридизацией образует солеобразные соединения 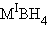 .
.



