 Модель 4.4.
Изохорный процесс
Модель 4.4.
Изохорный процесс Модель 4.4.
Изохорный процесс
Модель 4.4.
Изохорный процесс |
Моделируется процесс изохорного нагревания и охлаждения идеального газа. Текущие значения параметров газа выводятся на экран. Состояние газа указывается на графике в координатах (
Изохорный процесс – это процесс квазистатического нагревания или охлаждения вещества (в данном случае идеального газа) при постоянном объеме
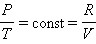 ,
,
|
В изохорном процессе газ не совершает работы:
Первый закон термодинамики для изохорного процесса записывается в виде
При изохорном нагревании тепло поглощается газом (
В модели можно выбирать объем газа и проводить процесс при разных объемах газа.
Приведен график зависимости
Из энергетической диаграммы видно, что при изохорном процессе работа газа равна нулю, и все полученное тепло затрачивается на изменение внутренней энергии газа.



