 Модель 6.4.
Полунепроницаемая мембрана
Модель 6.4.
Полунепроницаемая мембрана Модель 6.4.
Полунепроницаемая мембрана
Модель 6.4.
Полунепроницаемая мембрана |
Моделируется процесс возникновения осмотического давления в системе с полупроницаемой перегородкой. Перегородка, разделяющая сосуд на две половины, проницаема для одного из газов и непроницаема для другого. Модель позволяет продемонстрировать закон Дальтона для смеси газов.
Если в сосуде находится смесь газов, то каждый из них вносит свой вклад в общее давление. Парциальным давлением называют давление одного из газов при условии, что все остальные удалены из сосуда. Экспериментально установленный закон Дальтона утверждает: давление в смеси химически невзаимодействующих газов равно сумме их парциальных давлений:
При этом парциальное давление каждого из газов подчиняется в случае достаточно разреженных газов уравнению состояния идеального газа:
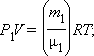 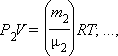 |
Примером газовой смеси является воздух, состоящий из азота, кислорода, углекислого газа и других газов.
Иллюстрацией закона Дальтона может служить процесс диффузии газа через полупроницаемую перегородку (мембрану). Пусть в начальный момент два разных газа занимают две половины сосуда, разделенные полупроницаемой мембраной. Температуры обоих газов и их начальные давления одинаковы. Мембрана полностью непроницаема для одного из газов и частично прозрачна для другого. В процессе диффузии газа через полупроницаемую перегородку давление в одной половине сосуда возрастает в соответствии с законом Дальтона, а в другой – падает. Это явление носит название осмоса.



