|
История открытия электрона |  |
 |

|
Американский ученый и политический деятель Бенджамин Франклин в середине XVIII века занимался исследованием электрических явлений и создал азбуку электрических терминов. Он ввел в жизнь такие термины, как заряд, батарея, конденсатор, проводник, разряд, обмотка, отрицательный и положительный заряды. Английский ученый Майкл Фарадей в 1833 году обнаружил, что при электролизе любого одновалентного вещества выделение одного моля вещества у одного электрода сопровождается переносом одного и того же количества электричества, равного
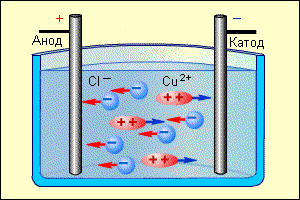
М. Фарадей установил, что ток в растворе электролита — это упорядоченное движение заряженных частиц — ионов. Фарадей определил минимальный заряд иона, который был назван элементарным электрическим зарядом. Его приближенное значение оказалось равным Имя Фарадея увековечено и в названии единицы электрической емкости. Постоянная Фарадея численно равна заряду, который необходимо пропустить через электролит для выделения на электроде одного моля одновалентного вещества.
где
Томас Эдисон в 1883 году обнаружил явление термоэлектронной эмиссии, при которой катод, нагретый до высокой температуры, может испускать электроны. В газах при больших напряженностях электрических полей электроны приобретают большую энергию.
Французский физик Жан Перрен в 1895 году обнаружил, что катодные лучи являются потоком частиц с отрицательным зарядом. Английский физик Джозеф Томсон в 1897 году открыл электрон и измерил отношение Таким образом, на основании всех известных к началу XX века экспериментальных фактов можно было сделать вывод о том, что атомы вещества имеют сложное внутреннее строение. Они представляют собой электрически нейтральные системы, причем носителями отрицательного заряда в атомах являются легкие электроны, масса которых составляет лишь малую долю массы атомов. Основная часть массы атомов связана с положительным зарядом. |