|
|||||||||||||||||||||||||
|
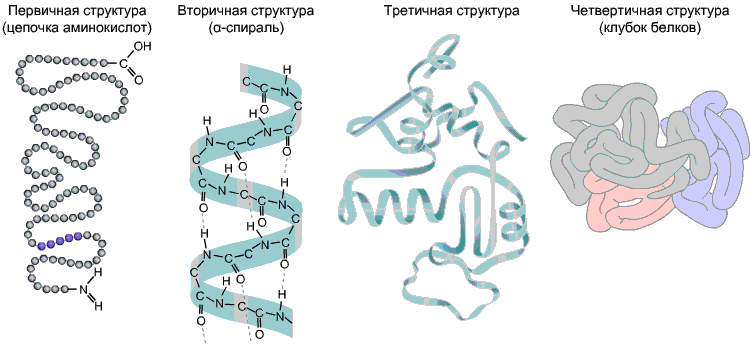
В молекуле белка аминокислотные остатки соединены так называемой пептидной связью. Полная последовательность аминокислотных остатков в такой цепи называется первичной структурой белка. Число остатков в разных белках может колебаться от нескольких штук до нескольких тысяч. Небольшие молекулы с мол. массой менее 10 тыс. дальтон называют пептидами, а крупные – белками. В составе белка обычно имеются как кислые, так и щелочные аминокислоты, так что белковая молекула имеет и положительные, и отрицательные заряды. Значение рН, при котором количество отрицательных зарядов равно количеству положительных, называется изоэлектрической точкой белка.
Обычно белковая цепочка складывается в более сложные структуры. Кислород группы C=O может образовывать водородную связь с водородом группы N–H, расположенной в другой аминокислоте. За счет таких водородных связей формируется вторичная структура белка. Одна из разновидностей вторичной структуры – α-спираль. В ней каждый кислород С=О-группы связан с водородом 4-й по ходу спирали NH-группы. На один виток спирали приходится 3,6 аминокислотных остатка, шаг спирали составляет 0,54 нм.
Во многих белках имеется т. н. β-структура, или β-слой, в ней полипептидные цепочки почти полностью развернуты, их отдельные участки своими группами –СО– и –NH– образуют водородные связи с другими участками той же цепочки или соседней полипептидной цепи. α-Спиральную структуру имеет белок кератин, из которого состоят волосы и шерсть. При нагревании влажные волосы и шерсть легко поддаются растяжению, а потом самопроизвольно возвращаются к исходному состоянию: при растяжении водородные связи α-спирали разрываются, а затем постепенно восстанавливаются. β-Структура характерна для фиброина – основного белка шелка, выделяемого гусеницами шелкопряда. В отличие от шерсти, шелк почти нерастяжим – β-структура образована вытянутыми полипептидными цепями, и дальше растягивать ее практически невозможно без разрыва ковалентных связей. Укладка белков обычно не ограничивается вторичной структурой. Гидрофобные аминокислотные остатки «стремятся» укрыться от водного окружения внутри белковой молекулы. Между боковыми группами кислых и щелочных аминокислот, заряженных, соответственно, отрицательно и положительно, возможно электростатическое взаимодействие. Многие аминокислотные остатки могут образовывать друг с другом водородные связи. Наконец, остатки аминокислоты цистеина, содержащие SH-группы, способны образовывать между собой ковалентные связи –S–S–. Благодаря всем этим взаимодействиям – гидрофобным, ионным, водородным и дисульфидным – белковая цепочка образует сложную пространственную конфигурацию, называемую третичной структурой. В составе глобулы у многих белков можно различить отдельные компактные участки размером около 10–20 тысяч дальтон. Они называются доменами. Участки полипептидной цепи между доменами весьма гибки, так что всю структуру можно представить как относительно жесткие бусины доменов, соединенные гибкими промежуточными участками первичной структуры. Многие белки (их называют олигомерными) состоят не из одной, а из нескольких полипептидных цепочек. Совокупность их образует четвертичную структуру белка, при этом отдельные цепочки называются субъединицами. Четвертичная структура удерживается теми же связями, что и третичная. Пространственная конфигурация белка (т. е. его третичная и четвертичная структура) называется конформацией.
Главным методом, позволяющим устанавливать пространственную структуру белков и других биологических полимеров, является рентгеноструктурный анализ. В последнее время большие успехи достигнуты в компьютерном моделировании белковых конформаций. Водородные, электростатические и гидрофобные связи, с помощью которых создаются вторичная, третичная и четвертичная структуры белка, менее прочны, чем пептидная связь, образующая первичную структуру. При нагревании они легко разрушаются, и хотя у белка сохраняется в целости первичная структура, он не может выполнять своих биологических функций, становится неактивным. Процесс разрушения природной конформации белка, сопровождающийся потерей активности, называется денатурацией. Денатурацию вызывает не только нагревание, но и химические вещества, нарушающие связи вторичной и третичной структур – например, мочевина, которая в высоких концентрациях разрушает водородные связи в белковой глобуле. Дисульфидные –S–S-связи образуют прочные «скрепы», сшивающие различные участки одной полипептидной цепи или разные цепи. Эти связи имеются, например, в кератинах, причем разные кератины содержат разное количество таких сшивок: волосы и шерсть – немного, рога, копыта млекопитающих и панцири черепах – значительно больше. Вторичная, третичная и четвертичная структура белка определяется его первичной структурой. В зависимости от последовательности аминокислот в полипептидной цепочке будут образовываться α-спиральные или β-структурные участки, которые затем самопроизвольно «уложатся» в определенную третичную структуру, а у некоторых белков отдельные цепочки еще и объединятся с образованием четвертичной структуры. Если изменить первичную структуру белка, то может сильно измениться и вся его конформация. Существует тяжелая наследственная болезнь – серповидно-клеточная анемия, при которой гемоглобин становится малорастворим в воде, а эритроциты приобретают серповидную форму. Причина болезни – замена всего лишь одной аминокислоты из 574, входящих в состав человеческого гемоглобина (глютаминовая кислота, расположенная на 6-м месте с N-конца одной из цепей гемоглобина нормальных людей, у больных заменена на валин). Процесс самопроизвольной ассоциации белковых субъединиц в сложные комплексы, обладающие четвертичной структурой, называется самосборкой. Большинство белковых комплексов с четвертичной структурой образуются именно путем самосборки.
В 1980-е годы было обнаружено, что не все белки и белковые комплексы образуются путем самосборки. Оказалось, что для образования таких структур как нуклеосомы (комплексы белков-гистонов с ДНК), бактериальные ворсинки – пили, а также некоторых сложных ферментных комплексов используются специальные белки–помощники, названные шаперонами. Шапероны не входят в состав образующейся структуры, а только помогают ее укладке. Шапероны служат не только для организации сложных комплексов, но в некоторых случаях помогают правильно свернуть одну полипептидную цепочку. Так, при воздействии высокой температуры в клетках резко возрастает количество т. н. белков теплового шока. Они связываются с частично денатурированными клеточными белками и восстанавливают их природную конформацию.
Долгое время считалось, что белок может иметь только одну устойчивую конформацию при данных условиях, но в последнее время этот постулат пришлось пересмотреть. Поводом к такому переосмыслению послужило открытие возбудителей т. н. медленных нейрологических инфекций. Эти инфекции встречаются у разных видов млекопитающих. К ним относится болезнь овец «скрепи», заболевание человека «куру» («смеющаяся смерть») и нашумевшее в последнее время «бешенство коров». Они имеют много общего. Для них характерны тяжелые поражения центральной нервной системы. Так, люди, больные куру, на ранних стадиях болезни испытывают эмоциональную неустойчивость (большинство – часто и беспричинно смеются, но некоторые находятся в состоянии депрессии или немотивированной агрессивности) и легкие нарушения координации движений. На поздних стадиях больные уже не способны не только двигаться, но даже сидеть без поддержки, а также есть. Заражение обычно происходит пищевым путем (изредка через кровь). Болезнь у животных развивалась после скармливания им костной муки, которая изготавливалась из костей больных особей. Куру – болезнь папуасских людоедов, передающаяся при поедании мозга умерших родичей (поедание друг друга в этом случае – скорее отрасль богослужения, чем кулинарии, оно имеет важное ритуальное значение). Все эти заболевания имеют очень длительный инкубационный период и развиваются медленно. В головном мозге заболевших отмечается отложение нерастворимого белкового конгломерата. Нерастворимые белковые нити обнаруживаются в пузырьках, расположенных внутри нейронов, а также во внеклеточном веществе. Наблюдается разрушение нейронов в некоторых отделах мозга, особенно в мозжечке. Долгое время оставалась загадочной природа возбудителей этих заболеваний, и только в начале 80-х годов было установлено, что эти возбудители – особые белки с молекулярной массой около 30 тысяч дальтон. Такие доселе неизвестные науке объекты получили название прионы. Было установлено, что прионный белок закодирован в ДНК организма-«хозяина». Белок здорового организма содержит ту же последовательность аминокислот, что и белок инфекционной частицы приона, но никаких патологических симптомов не вызывает. Функция прионного белка пока неизвестна. Мыши, у которых генные инженеры искусственно выключили ген этого белка, развивались вполне нормально, хотя и имели некоторые отклонения в работе центральной нервной системы (худшее обучение, нарушения сна). В здоровом организме этот белок обнаружен на поверхности клеток во многих органах, больше всего в головном мозге. Оказалось, что в инфекционной частице прионный белок имеет иную конформацию, чем в нормальных клетках. Он содержит бета-структурные участки, обладает высокой устойчивостью к расщеплению пищеварительными ферментами и способностью образовывать нерастворимые агрегаты (видимо, отложение таких агрегатов в мозге и является причиной развития нейропатологии).
Самое интересное, что «нормальная» конформация этого белка превращается в «болезнетворную», если клетка контактирует с «болезнетворным» белком. Получается, что «болезнетворный» белок «лепит» пространственную структуру «нормального» по себе. Он направляет его укладку как матрица, вызывая появление все большего числа молекул в «болезнетворной» конформации и, в конце концов, гибель организма.
Как именно это происходит, до сих пор неизвестно. Если смешать в пробирке нормальную и инфекционную форму прионного белка, то никакого образования новых инфекционных молекул не произойдет. По-видимому, в живой клетке имеются какие-то молекулы-помощники (вероятно, шапероны), позволяющие прионному белку делать свое черное дело.
Отложение нерастворимых белковых конгломератов может служить причиной и других неизлечимых нервных заболеваний. Болезнь Альцгеймера не относится к числу инфекционных – она возникает в пожилом и старческом возрасте у людей с наследственной предрасположенностью. У больных наблюдается ухудшение памяти, ослабление интеллекта, слабоумие, и, в конце концов – полная утрата психических функций. Причина развития болезни – отложение в мозгу т. н. амилоидных бляшек. Они состоят из нерастворимого белка – β-амилоида. Он представляет собой фрагмент белка–предшественника амилоида – нормального белка, присутствующего у всех здоровых людей. У больных он расщепляется с образованием нерастворимого амилоидного пептида. Мутации в разных генах вызывают развитие болезни Альцгеймера. Естественно, ее вызывают мутации в гене белка–предшественника амилоида – измененный предшественник после расщепления образует нерастворимый β-амилоид, формирующий бляшки и разрушающий клетки головного мозга. Но болезнь возникает и при мутации в генах белков, регулирующих активность протеаз, разрезающих белок – предшественник амилоида. Не совсем понятно, как в этом случае развивается заболевание: возможно, нормальный белок предшественник режется в каком-то неправильном месте, что приводит к выпадению в осадок образующегося пептида. Очень рано болезнь Альцгеймера развивается у больных с синдромом Дауна – у них содержится не две копии 21-й хромосомы, как у всех людей, а три. Больные синдромом Дауна имеют характерную внешность и слабоумие. Дело в том, что ген белка–предшественника амилоида как раз и находится в 21-й хромосоме, увеличение количества гена приводит к увеличению количества белка, а избыток белка–предшественника приводит к накоплению нерастворимого β-амилоида.
Белки часто соединяются с другими молекулами. Так, гемоглобин, переносящий кислород в кровеносной системе, состоит из белковой части – глобина, и небелковой – гема. Ион Fe2+ входит в состав гема. Глобин состоит из четырех полипептидных цепочек. Благодаря наличию гема с железом гемоглобин катализирует окисление перекисью водорода различных органических веществ – например, бензидина. Раньше эта реакция под названием «бензидиновая проба» использовалась в судебно-медицинской экспертизе для обнаружения следов крови. Некоторые белки химически связаны с углеводами, их называют гликопротеины. Очень многие белки, секретируемые животной клеткой, являются гликопротеинами – например, известные по предыдущим разделам трансферрин и иммуноглобулины. Однако, желатин, хотя и является продуктом гидролиза секретируемого белка коллагена, практически не содержит присоединенных углеводов. Внутри клетки гликопротеины встречаются гораздо реже. В лабораторной практике используется много методов определения концентрации белка. В самом простом из них применяется биуретовый реактив – щелочной раствор соли двухвалентной меди. В щелочной среде некоторая часть пептидных связей в молекуле белка переходит в енольную форму, которая образует с двухвалентной медью комплексы, окрашенные в красный цвет. Другой распространенной реакцией на белок является окраска по Бредфорду. В ходе реакции молекулы специального красителя связываются с белковой глобулой, что вызывает резкое изменение окраски – из бледно-коричневого раствор становится ярко-синим. Это краситель – «кумасси ярко-синий» – раньше использовался для окраски шерсти (а шерсть, как известно, состоит из белка кератина). Наконец, для определения концентрации белка можно использовать его свойство поглощать ультрафиолетовый свет с длиной волны 280 нм (его поглощают ароматические аминокислоты фенилаланин, тирозин и триптофан). Чем сильнее раствор поглощает такой ультрафиолет, тем больше там содержится белка.
Краткое содержание урока
|