|
|||||||||||||||||||||||||
|
Для того чтобы изучать свойства и функции определенного соединения в живых организмах (например, какого-то конкретного белка), необходимо выделить его в чистом виде. Однако в живых клетках и тканях имеется огромное количество разных белков и других органических соединений. В биохимии используются различные методы для разделения этих сложных смесей. До сих пор широко используются способы разделения, основанные на различиях в растворимости веществ. Так, липиды хорошо растворяются в гидрофобных растворителях – хлороформе, эфире и др., тогда как белки, углеводы и другие гидрофильные вещества в них не растворимы. В свою очередь разные белки имеют различную растворимость в смесях воды и органических растворителей (спирта, ацетона др.) с разной концентрацией. Все белки плохо растворимы в растворах с очень низким рН, например, в 1 М HClO4, что позволяет осаждать их из биологических смесей, однако при этом происходит необратимая денатурация белков. Более мягким, не повреждающим способом является высаливание – осаждение белка высокими концентрациями солей, как правило, сульфатом аммония. Однако кривые растворимости многих белков проходят близко друг к другу, и чисто разделить их таким способом не удается. Как правило, высаливание применяется на ранних этапах очистки, а для последующего тонкого разделения применяются другие методы. Одним из таких методов является хроматография. В ее основе лежит использование специальных нерастворимых матриц-сорбентов, способных связывать различные вещества из раствора. Принцип разделения состоит в том, что разные вещества из сложных биологических смесей имеют разное сродство к этому нерастворимому сорбенту. При промывании такой матрицы растворителем вещества с низким сродством к сорбенту будут вымываться первыми, с более высоким – вторыми и т. д.
Существует несколько разновидностей хроматографии – адсорбционная, ионообменная и др. Сам метод был изобретен русским ученым М. С. Цветом. Он разделял растительные пигменты (хлорофиллы и каротиноиды) на основе их различного сродства к порошку мела. Пигменты образовывали на колонках с мелом цветные полоски с разной окраской, что и позволило назвать метод хроматографией (по-гречески χρωμα означает «цвет», по другой версии метод получил название по фамилии изобретателя). Этот вид хроматографии называется адсорбционной – разделяемые вещества сорбируются на носителе благодаря ван-дер ваальсовым силам (их природа здесь не рассматривается, про них можно прочитать в учебниках физики). Недостатком адсорбционной хроматографии является невозможность предсказать, какое вещество прочнее свяжется с сорбентом, а какое слабее, это приходится устанавливать опытным путем. Для проведения ионообменной хроматографии используют ионообменники. Это нерастворимые в воде гранулы, на поверхности которых имеются электрические заряды. В качестве примера можно привести карбоксиметилцеллюлозу. Для ее получения гранулы обычной целлюлозы размером 40–80 микрон обрабатывают таким образом, что часть гидроксильных групп превращается в карбоксильные. В водной среде они диссоциируют, отдавая ион H+: R–COOH ↔ R–COO– + H+ Допустим, у нас имеется смесь трех белков с изоэлектрическими точками 5,5; 6,5 и 7,5. При рН 5 все они будут иметь положительный заряд и связываться с ионообменником за счет электростатических сил. Если повысить рН до 5,5, то первый белок достигнет изоэлектрической точки, перестанет связываться с карбоксиметилцеллюлозой, и его можно будет отделить от остальных белков. Если после этого поднять рН до 6,5, то с ионообменника будет удален второй белок, а третий можно удалить, повысив рН до 7,5. Снимать белки с ионообменника можно изменением не только рН, но и концентрации ионов в растворе. При рН 5 у первого белка будет наименьший заряд, и он связывается с карбоксиметилцеллюлозой слабее других. Если добавить к ионообменнику раствор KCl невысокой концентрации, то ионы K+ будут вытеснять первый белок, а второй и третий при этом еще будут связаны с ионообменником. При дальнейшем повышении концентрации KCl можно удалить второй белок, а затем и третий. Для проведения хроматографии используют также и анионообменники. Практически ионообменную хроматографию проводят следующим образом. Суспензию гранул ионообменника наливают в специальный цилиндрический сосуд – колонку. На дне колонки есть отверстие, а над ним расположена мелкопористая сетка, через которую не проходят гранулы, но свободно протекают растворы. Суспензии дают осесть и промывают, пропуская через колонку соответствующий раствор. Затем наносят смесь разделяемых веществ (например, белков) и проводят отмывку от несвязавшихся с ионообменником. Наконец, последовательно пропуская растворы с различной ионной силой и разным рН, снимают с колонки нужные белки. Ионообменная хроматография позволяет разделять вещества по электрическому заряду. Другой метод, гель-проникающая хроматография, служит для разделения различных молекул по молекулярной массе и размеру. Для гель-проникающей хроматографии колонку заполняют суспензией гранул, в которых имеются поры определенных размеров. Обычно это гранулы нерастворимого полисахарида декстрана. Крупные молекулы не могут заходить в поры этих гранул, а мелкие – могут. Если на колонку нанести смесь белков разной молекулярной массы, а затем пропускать через нее промывающий раствор, то самые крупные белки, не входящие в поры, почти не будут задерживаться в колонке и выйдут первыми. Молекулы с меньшей молекулярной массой будут задерживаться в колонке, диффундируя внутрь гранул. Чем меньше молекулярный вес белка, тем позже он выйдет с колонки.
Жидкость, вытекающую из колонки и содержащую разделенные белки, собирают в отдельные пробирки. Содержание белка там определяют с помощью специфических реакций или измеряя поглощение ультрафиолета (см. урок 5). Существуют специальные анализаторы, которые измеряют поглощение ультрафиолетового света прямо в токе жидкости, стекающей с колонки, и регистрируют его с помощью самописца. С их помощью можно каждый выходящий из колонки белок собрать в отдельную пробирку. Для проведения хроматографии не обязательно использовать колонку. Можно нанести тонкий слой сорбента на плоскую пластинку и закрепить его там (например, специальным клеем). Небольшое количество исследуемого образца наносят на пластинку, высушивают, и помещают эту пластинку в специальную камеру, на дно которой налито немного растворителя. Благодаря капиллярным силам раствор элюента поднимается вверх по пористой пластинке. При этом разные химические вещества, содержащиеся в нанесенных образцах, имеют различное сродство к сорбенту, «цепляются» за него с разной силой и поэтому движутся с разной скоростью. Как только фронт растворителя дойдет почти до верхнего края, пластинку вынимают и высушивают. Для обнаружения разделившихся веществ пластинку обрабатывают специфическими красителями (например, для обнаружения аминокислот – нингидрином). Разные вещества при этом оказываются на различных расстояниях от точки нанесения, что позволяет идентифицировать их. Этот вариант метода получил название тонкослойной хроматографии. Обычно тонкослойную хроматографию применяют для анализа небольших количеств веществ, а колоночную – для обработки больших препаратов. Чаще всего используют пластинки с носителем для адсорбционной хроматографии (SiO2 или Al2O3 или целлюлозой), иногда – ионообменной.
Еще один метод разделения биологических веществ – электрофорез. В основе его лежит движение молекул в электрическом поле. В ранних вариантах метода биологические смеси наносили на бумажную полоску, пропитанную буферным раствором, и присоединяли концы полоски к катоду и аноду. Под действием электрического поля разные молекулы двигались в разных направлениях и с разными скоростями. Направление движения молекул определялось знаком суммарного заряда молекулы данного вещества при выбранном рН буферного раствора, а скорость движения – величиной этого заряда. После того, как самое «быстрое» вещество дойдет до конца полоски, электрический ток выключали, и вещества с различным зарядом молекулы оказывались в разных участках бумажной полоски.
Количество смеси веществ, которое можно разделить с помощью электрофореза, обычно бывает невелико, поэтому данный метод чаще используют для анализа, а не для препаративного выделения нужного вещества. Электрофорез на бумаге сейчас не используется, его заменил более современный вариант – электрофорез в геле. По своей консистенции гель похож на студень или на мармелад: это твердое эластичное вещество, состоящее из длинных нитей полимера, между которыми свободно перемещается вода и небольшие ионы. Электрофорез часто проводят в гелях агарозы – полисахарида, похожего по свойствам на крахмал, но состоящего из других моносахаридов и неразветвленного. Гранулы агарозы образуют в водных растворах суспензию. При нагревании почти до кипения водородные связи между молекулами агарозы разрываются, и она растворяется. Раствор агарозы выливает на пластинку и дают остыть. При понижении температуры вновь образуются водородные связи между молекулами агарозы, и раствор превращается в студнеобразный гель (сравните с водными растворами крахмала, см. урок 3). Агарозные гели часто применяют для разделения нуклеиновых кислот, а белки чаще разделяют в полиакриламидном геле. Акриламид CH2=CH–CO–NH2 представляет собой соединение, способное полимеризоваться. Полимер, образованный из остатков акриламида,
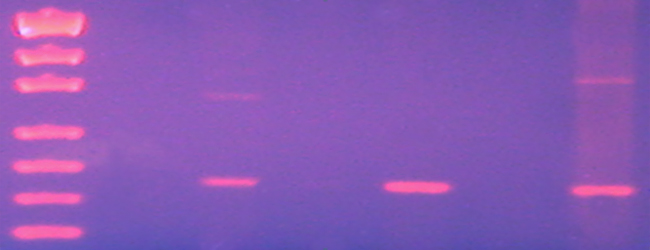
К краям пластинки с гелем присоединяют катод и анод и включают электрический ток. Под действием электрического поля молекулы будут двигаться в соответствии со своим зарядом. Следует отметить, что при электрофорезе в геле происходит разделение макромолекул не только по заряду, но и по размеру молекулы. Полимерные цепочки геля образуют пространственную решетку, через которую приходится «протискиваться» белкам и нуклеиновым кислотам. Крупные молекулы будут часто ударяться об эту решетку, что сильно замедлит их движение, молекулы среднего размера будут ударяться не так часто, и эффект замедления скажется меньше, а мелкие молекулы почти не будут ударяться о решетку. Для того чтобы следить за протеканием электрофореза, к разделяемой смеси обычно добавляют специальный лидирующий краситель – вещество, которое будет двигаться быстрее самой быстрой макромолекулы. Как только он дойдет до конца пластинки геля, ток выключают. Для того чтобы увидеть результаты электрофореза, существует несколько способов. После проведения электрофореза ДНК гель вымачивают в растворе бромистого этидия. Молекулы этого вещества встраиваются между парами азотистых оснований в двойную спираль ДНК. Если теперь осветить ДНК ультрафиолетом, то бромистый этидий будет флуоресцировать – светиться оранжевым светом. Светящиеся оранжевые полоски представляют собой молекулы двухцепочечной ДНК разного размера.
Для белков применяют другой способ. Гель обрабатывают красителем, молекулы которого связываются с белковой глобулой (обычно это кумасси ярко-синий, о котором говорилось на 5-м уроке). После этого гель отмывают от несвязавшегося красителя, и окрашенные полоски белка становятся хорошо видимы невооруженным глазом. Для того чтобы увидеть местоположение ферментов в геле, применяют окраску по активности. Гель вымачивают в растворе, содержащем субстрат интересующего нас фермента. Субстрат берут не любой, а такой, чтобы в ходе ферментативной реакции давал нерастворимый окрашенный продукт. В результате в тех местах геля, где есть исследуемый фермент, появятся полоски окрашенного продукта. Для диагностики целого ряда заболеваний применяют электрофорез сыворотки крови с последующей окраской на фермент лактатдегидрогеназу. У здоровых людей в крови преобладает 2-я изоформа этого фермента, у больных инфарктом миокарда при разрушении сердечной мышцы в кровь выходит много 1-й изоформы, а у больных гепатитом из погибших клеток печени освобождается много 4-й и 5-й изоформ. Существует вариант метода электрофореза в геле, позволяющий разделять белки строго по молекулярной массе, без всякого влияния изоэлектрической точки – это электрофорез в додецилсульфате натрия (ДДС). ДДС После обработки ДДС белковая молекула приобретает отрицательный заряд, причем, чем крупнее белок, тем заряд больше. Соотношение заряда к массе у всех белков становится одинаковым, и теперь скорость их движения зависит только от трения о пространственную решетку геля. Оно определяется размерами белка: чем крупнее белок, тем медленнее он будет двигаться в геле. К сожалению, обработка ДДС вызывает денатурацию белковых молекул и необратимую потерю ферментативной активности. В противоположность электрофорезу с ДДС, еще один метод – изоэлектрофокусировка – разделяет белки только по их изоэлектрическим точкам. Принцип метода состоит в том, что в гель добавляют особые вещества – амфолиты. Это небольшие амфотерные молекулы с мол. массой несколько сотен дальтон. У них есть ценное для биохимиков свойство: под действием электрического поля эти вещества создают градиент рН – около катода среда будет щелочной, около анода – кислой, а по ходу геля рН будет плавно меняться. Допустим, молекула определенного белка оказалась в зоне с рН выше его изоэлектрической точки. Она приобретет отрицательный заряд и будет двигаться к аноду. В процессе движения она будет попадать в области со все более низким рН и наконец дойдет до участка, где рН равен изоэлектрической точке. Там молекула белка остановится, поскольку ее суммарный заряд будет равен нулю. Пусть другая молекула оказалась в зоне с рН ниже изолектрической точки. У нее будет положительный заряд, она станет двигаться к катоду и тоже дойдет до зоны с рН, равным изоэлектрической точке. В итоге все молекулы данного белка сконцентрируются в очень узкой области, соответствующей его изоэлектрической точке. Другой белок будет сосредотачиваться в другой зоне, третий – в третьей и т. д. Для проведения изоэлектрофокусировки используют самые крупнопористые гели, чтобы трение о пространственную решетку не замедляло движение белков. Если хотят разрушить четвертичную структуру белков и разделить их на субъединицы, то в гель добавляют мочевину.
Изоэлектрофокусировка разделяет белки по изоэлектрическим точкам, а электрофорез в додецилсульфате натрия – по молекулярной массе. Самое лучшее разделение получается при сочетании этих методов – двумерном электрофорезе. Белковую смесь сперва подвергают изоэлектрофокусировке. Затем полоску геля вымачивают в растворе додецилсульфата натрия, накладывают на пластину полиакриламидного геля с ДДС и проводят электрофорез в направлении, перпендикулярном направлению изоэлектрофокусировки. В результате белки будут находиться в виде маленьких пятнышек на пластинке геля – получится как бы двумерная карта всех белков данной смеси. При этом «долгота» белкового пятнышка определяется его изоэлектрической точкой, а «широта» – его молекулярной массой.
Двумерный электрофорез позволяет провести разделение всех белков, содержащихся в живой клетке. В последнее время бурно развивается протеомика – область биохимии, изучающая весь спектр белков в каждом типе тканей, а также изменения этого спектра в норме (например, при увеличении функциональной нагрузки) и при патологии (например, при опухолевой трансформации). Протеомика позволит глубже понять причины различных патологических состояний организма и разработать новые способы их лечения. Метод двумерного электрофореза играет важнейшую роль в исследованиях, посвященных протеомике. К настоящему времени полностью расшифрована последовательность нуклеотидов во всей ДНК человека, определено число генов, кодирующих белки (см. урок 7). Однако непосредственные фенотипические проявления организма определяют белки, а не нуклеиновые кислоты (в подавляющем большинстве случаев). Число же разных форм белков значительно превышает число генов – мы уже говорили, что один и тот же белок может по-разному фосфорилироваться, по-разному укладываться, по-разному разрезаться (см. уроки 5 и 6). По некоторым подсчетам общее число белковых форм может достигать нескольких сотен тысяч. Так что задачи, стоящие перед протеомикой, поистине грандиозны, однако и перспективы развития этого научного направления весьма заманчивы: энтузиасты протеомики полагают, что полная информация о белковом спектре клетки даст возможность познать все сферы ее жизнедеятельности и научиться управлять ими. Правда, скептики считают, для этого понадобятся еще и новые великие теории, ибо груда кирпичей сама по себе не складывается в красивое здание. Кто из них прав, покажет время.
Краткое содержание урока
|