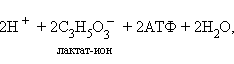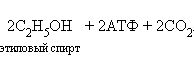|
|||||||||||||||||||||||||||||||
|
Катаболизм органических соединений в организме животных протекает в три стадии. На первой из них происходит распад сложных веществ, поступающих с пищей, на более простые фрагменты: углеводы гидролизуются до моносахаридов, белки до аминокислот, жиры – до глицерина и жирных кислот. Этот этап протекает внеклеточно в пищеварительной системе. Вся энергия, освобождающаяся в ходе этого процесса, рассеивается в виде тепла. Затем продукты первого этапа поступают в кровеносную систему и разносятся к различным органам и тканям, где они подвергаются последующим превращениям уже внутри клеток – потребителей энергии. На втором этапе происходит дальнейшее расщепление этих веществ без участия кислорода, в итоге образуется очень небольшой набор промежуточных метаболитов. Одни реакции второго этапа протекают в цитоплазме – катаболизм сахаров, некоторых аминокислот и глицерина. Другие идут в митохондриях – катаболизм жирных кислот и некоторых аминокислот. В некоторых реакциях этого этапа энергия расщепления органических веществ преобразуется в энергию АТФ – это происходит в ходе катаболизма моносахаридов и глицерина. В остальных же случаях энергия теряется в виде тепла. Наконец, на третьем этапе происходит окисление промежуточных метаболитов второго этапа. Третий этап протекает исключительно в митохондриях, он сопровождается поглощением кислорода. Именно на третьем этапе происходит выделение основного количества энергии, запасенной в пище и синтезируется большая часть АТФ для нужд животной клетки.
Реакции первого этапа катализируются пищеварительными ферментами желудочно-кишечного тракта, и здесь подробно рассматриваться не будут. Из реакций второго этапа одним из самых древних метаболических путей является гликолиз. Гликолиз может протекать в двух вариантах – аэробном (с участием кислорода) и анаэробном (бескислородном), они различаются лишь последней реакцией этого процесса. Аэробный гликолиз будет рассмотрен на следующем уроке. Анаэробный гликолиз не требует наличия свободного кислорода. Считается, что анаэробный гликолиз уже существовал на очень ранних этапах эволюции жизни на Земле, когда кислород в атмосфере еще отсутствовал. Гликолиз является наиболее распространенным метаболическим путем анаэробного синтеза АТФ. В самом общем виде уравнение этого процесса выглядит следующим образом:
На самом деле, правильнее было бы написать уравнение гликолиза в виде:
поскольку в нейтральной среде молочная кислота диссоциирует до лактат-иона. Анаэробный гликолиз в клетках бактерий носит название молочнокислого брожения. Гликолиз – не единственный пример анаэробного синтеза АТФ. Дрожжи используют другую реакцию – спиртовое брожение:
И молочнокислое, и спиртовое брожение протекают в цитоплазме клеток. Известны и другие типы брожений, используемых различными микроорганизмами: пропионовокислое, маслянокислое и др. Начальные этапы всех этих реакций брожения одинаковы, они различаются лишь на самых последних этапах. Различные виды брожений, осуществляемых микроорганизмами, давно используются человеком в своей хозяйственной деятельности. Молочнокислое брожение дает нам такие продукты как простокваша, йогурт (делаются из цельного молока), ряженка (изготавливается из топленого молока) и сметана (из сливок). Различные виды молочнокислых бактерий образуют продукты со своим специфическим вкусом. Осаждающиеся при закислении среды в ходе брожения белки молока образуют творог. Если осадить белки молока с помощью специальных протеаз, а затем подвергнуть осадок молочнокислому брожению, то получится сыр. Квашение капусты также протекает с участием молочнокислых бактерий. Такие продукты как квас, кефир и кумыс получаются в результате идущих одновременно молочнокислого и спиртового брожений. Спиртовое брожение дает человечеству весь спектр алкогольных напитков. Пиво и столовое вино образуются непосредственно как продукт спиртового брожения, крепленые вина получаются после добавления спирта в столовые вина, а если сброженную жидкость перегнать, то можно приготовить крепкие напитки – водки, коньяки, бренди. Пропионовокислое брожение протекает в процессе изготовления швейцарского сыра, придавая этому продукту неповторимый вкус и аромат. При превращении глюкозы в молочную кислоту освобождается 47 ккал на моль, что вполне достаточно для синтеза двух молекул АТФ при катаболизме одной молекулы глюкозы. ногие клетки используют гликолиз как главный механизм синтеза АТФ – например, «быстрые» мышечные волокна скелетных мышц, участвующие в скоростных и силовых движениях, клетки молочнокислых бактерий и некоторые другие. Гликолиз представляет собой многоэтапный процесс, включающий 11 стадий.
На первых этапах гликолиза превращениям подвергаются шестиуглеродные сахара и их производные. В ходе самой первой реакции – гексокиназной – молекула глюкозы подвергается фосфорилированию, при этом затрачивается молекула АТФ. Может возникнуть вопрос: зачем природа пошла на такое расточительство? Почему почти все промежуточные соединения, участвующие в гликолизе, содержат фосфатную группу? Одна из важнейших причин состоит в том, что вещества, содержащие эту группу, не проникают через липидный бислой наружной мембраны. Ведь эта фосфатная группа заряжена, а ионы не могут проникнуть через гидрофобную сердцевину липидного бислоя без специальных переносчиков. Благодаря этому промежуточные метаболиты гликолиза не просачиваются из клетки наружу, и бессмысленная потеря этих веществ предотвращается. Глюкозо-6-фосфат легко изомеризуется во фруктозо-6-фосфат (2-я реакция). Он с затратой еще одной молекулы АТФ превращается во фруктозо-1,6-дифосфат, эта реакция (3-я) играет важную роль в регуляции скорости гликолиза, она катализируется ферментом фосфофруктокиназой. На этом этап шестиуглеродных сахаров заканчивается. На следующей стадии (4-й) происходит расщепление фруктозо-1,6-дифосфата на два трехуглеродных соединения: диоксиацетонфосфат и глицеральдегид-3-фосфат. Они легко переходят друг в друга с помощью фермента триозофосфатизомеразы: ДОАФ ↔ Г-3-Ф (5-я реакция). Поскольку глицеральдегид-3-фосфат вступает в дальнейшие превращения гликолиза и выводится из реакции, то в соответствии с принципом Ле-Шателье реакция будет протекать слева направо. В итоге из одной молекулы фруктозо-1,6-дифосфата получается две молекулы глицеральдегид-3-фосфата. Во всех дальнейших превращениях будут также участвовать по две молекулы трехуглеродных соединений из одной молекулы глюкозы. Следующая реакция гликолиза (6-я) является одной из важнейших. Это окислительно-восстановительная реакция, в ходе которой из глицеральдегид-3-фосфата образуется богатое энергией соединение 1,3-дифосфоглицериновая кислота. Если одно вещество окисляется (в данном случае альдегид окисляется до кислоты), то другое вещество должно восстанавливаться. В этой реакции восстанавливается особый кофермент, обозначаемый сокращенно НАД. Его полное название – никотинамидадениндинуклеотид. Данное вещество может существовать в двух формах: окисленной НАД+ и восстановленной НАД∙Н. Для превращения первой формы во вторую необходимо поступление двух электронов от окисляемого субстрата. В организме человека кофермент НАД синтезируется из никотиновой кислоты – витамина РР.
Источником электронов в нашем случае будет служить альдегидная группа глицеральдегид-3-фосфата. Однако реакция протекает сложнее, чем простое окисление альдегида в кислоту: ведь живой клетке необходимо получать энергию, а для этого нужны высокоэнергетические фосфаты. Поэтому в ходе реакции окисления глицеральдегид-3-фосфата происходит еще и присоединение неорганического фосфата.
Эта реакция может служить примером описанного на уроке 9 сопряжения экзергонической и эндергонической реакции. В самом деле, реакция окисления альдегида до кислоты:
идет самопроизвольно и сопровождается выделением энергии, а реакция присоединения фосфата к карбоксильной группе кислоты:
самопроизвольно идти не может. В живой клетке эти две реакции объединяются в одну, ее катализирует фермент глицеральдегид-3-фосфат-дегидрогеназа. Дегидрогеназами называют ферменты, катализирующие окисление своих субстратов не кислородом, а специальными коферментами (в данном случае таким коферментом является НАД+). Образовавшаяся 1,3-дифосфоглицериновая кислота содержит макроэргическую связь. Она даже более богата энергией, чем АТФ, поэтому легко может передать свой фосфат на АДФ, превращаясь в 3-фосфоглицериновую кислоту (7-я реакция гликолиза):
Вспомним, что из одной глюкозы образовалось два трехуглеродных фрагмента, так что и молекул АТФ тоже образуется две. На первых этапах было затрачено две молекулы АТФ, теперь эти энергозатраты возмещены. Однако пока еще никакой энергетической выгоды клетка не получила. С помощью еще двух реакций (8-й и 9-й) образуется фосфоенолпируват – самый богатый энергией макроэрг клетки (см. урок 9). Он легко может передать свой фосфат на АДФ, превратив его в АТФ (10-я реакция). Сам он при этом превращается в пировиноградную кислоту, которая при нейтральном рН диссоциирует, образуя пируват–ион:
Наконец-то процесс стал энергетически выгодным. В ходе гликолиза сначала затрачиваются 2 молекулы АТФ (1-я и 3-я реакции), но затем образуются 4 молекулы АТФ (7-я и 10-я реакции, в обеих участвуют двойное количество трехуглеродных метаболитов), так что общий баланс составляет +2 АТФ на 1 глюкозу. Однако процесс еще не закончен. В ходе 6-й реакции две молекулы кофермента НАД+ восстановились до НАД∙Н. Если бы конечным продуктом гликолиза был пируват, то очень скоро весь запас клеточного НАД+ исчерпался бы, и гликолиз не смог бы протекать дальше. Возникает проблема – куда девать восстановленный НАД∙Н? В процессе гликолиза на последней, 11-й реакции НАД∙Н восстанавливает пировиноградную кислоту до молочной, сам он при этом опять переходит в окисленную форму НАД+ (в нейтральной среде эти кислоты существуют в виде ионов – пирувата и лактата:
Интересно, что в разных органах содержатся разные формы фермента лактатдегидрогеназы, катализирующего эту реакцию, – у них разная первичная структура, они по-разному движутся при электрофорезе (см. урок 8). При повреждении органов и тканей фермент попадает в кровь. У здоровых людей в крови преобладает мышечная форма лактатдегидрогеназы – ведь скелетные мышцы все время работают и при этом немного повреждаются. У больных инфарктом миокарда преобладающей становится сердечная форма – из мертвых клеток сердечной мышцы. У больных гепатитом резко увеличено содержание печеночной формы. Измерение разных форм этого фермента используется в клинике для диагностики различных заболеваний. Итак, теперь процесс гликолиза закончен. Никотинамидный кофермент вернулся в исходное состояние, и снова может принимать участие в переработке глюкозы. Проблема утилизации восстановленного НАД∙Н стоит перед всеми анаэробными организмами. В разных типах брожения эта проблема решается по-разному. Спиртовое брожение отличается от молочнокислого тем, что пировиноградная кислота восстанавливается не до молочной кислоты, а до этилового спирта. Вместо 11-й, последней, реакции гликолиза у дрожжей в анаэробных условиях идут две другие. Сперва пировиноградная кислота превращается в уксусный альдегид с выделением углекислого газа.
Затем ацетальдегид восстанавливается до этилового спирта, при этом НАД∙Н окисляется до НАД+, эту реакцию катализирует фермент алкогольдегидрогеназа:
Интересно, что у человека тоже есть фермент алкогольдегидрогеназа, его природная функция неизвестна. При употреблении алкоголя именно этот фермент начинает его переработку и утилизацию. У некоторых людей активность алкогольдегидрогеназы очень низка, что является причиной длительного и сильного опьянения от небольших доз спиртных напитков. Уксусный альдегид, образующийся из этилового спирта, является токсичным веществом, он вызывает целый комплекс болезненных симптомов, в просторечье называемых похмельем. Ацетальдегид окисляется другим ферментом – альдегиддегидрогеназой. Пьяниц и алкоголиков лечат, давая им ингибиторы этого фермента – т. н. антабусы. После приема алкоголя у них накапливается уксусный альдегид, развивается долгое и мучительное похмелье, что, по идее, должно отвращать их от спиртных напитков. При других видах брожения превращения пировиноградной кислоты более сложные, мы их здесь рассматривать не будем. Во многих клетках имеются запасы глюкозы в виде полимера – гликогена. Для включения в катаболические процессы гликоген подвергается расщеплению, но не простому гидролизу (расщеплению водой), а фосфоролизу – расщеплению ионом неорганического фосфата. ЭЭту реакцию катализирует фермент гликогенфосфорилаза, мы говорили о нем в 6-м уроке:
Глюкозо-1-фосфат легко изомеризуется в глюкозо-6-фосфат специальным ферментом. Таким образом, если в гликолиз вступает гликоген, а не глюкоза, то процесс получается энергетически выгоднее: не нужно затрачивать АТФ для получения глюкозо-6-фосфата. Однако для синтеза гликогена клетке приходится затрачивать много энергии. В гликолиз легко могут войти другие шестиатомные сахара – галактоза и фруктоза – потребуются лишь дополнительные ферменты в самом начале этого метаболического пути. Ферменты усвоения этих сахаров есть у всех здоровых людей. Скорость гликолиза находится под строгим контролем – было бы глупо расходовать глюкозу просто так без необходимости. Среди многочисленных ферментов, участвующих в гликолизе, есть один, который катализирует самую медленную реакцию и таким образом определяет скорость всего процесса. Фермент, который определяет скорость какого-либо многостадийного процесса, называется ключевым ферментом. Оказалось, что ключевой фермент гликолиза – фосфофруктокиназа – ингибируется АТФ и активируется АДФ по аллостерическому механизму (см. урок 6). Когда в клетке концентрация АТФ низка, ключевой фермент работает «в полную силу», гликолиз идет с высокой скоростью, и образующийся при этом АТФ постепенно накапливается. Когда концентрация АТФ становится высокой, то ключевой фермент ингибируется. Скорость всего процесса гликолиза падает, что предотвращает бесполезный расход глюкозы. Таким образом, вся система работает в режиме автоматической регуляции: когда АТФ мало, с высокой скоростью идет процесс, приводящий к его синтезу, а когда АТФ становится много, он сам угнетает процесс своего образования. АДФ, образующийся при интенсивном расходе АТФ, действует противоположным образом, активируя фосфофруктокиназу и весь процесс гликолиза. Может возникнуть вопрос: а почему именно фосфофруктокиназа является ключевым ферментом гликолиза? Здесь сыграли свою роль несколько разных факторов. Регулировать лучше необратимую реакцию. Если заингибировать обратимую реакцию, то сперва это никак не отразится на скорости всего процесса. Ведь продукт обратимой реакции был в равновесии с ее исходным веществом, и только когда концентрация продукта сильно упадет, станет чувствоваться ее торможение. В гликолизе можно отметить три реакции, сопровождающиеся выделением большого количества энергии: гексокиназную (1-я), фосфофруктокиназную (3-я) и пируваткиназную (10-я). В физиологических условиях они практически необратимы, поскольку сопровождаются большим изменением свободной энергии Δ Активность всех трех ферментов, катализирующих необратимые реакции, регулируется. Гексокиназа аллостерически ингибируется своим конечным продуктом – глюкозо-6-фосфатом, а пируваткиназа – АТФ (в обоих случаях виден принцип отрицательной обратной связи). Казалось бы, на роль ключевого фермента лучше всего подходит гексокиназа, катализирующая самую первую реакцию гликолиза. Однако глюкозо-6-фосфат, продукт этой реакции, участвует не только в гликолизе, но и еще в нескольких метаболических путях. Если бы мы стали тормозить превращение глюкозы в глюкозо-6-фосфат, то ингибировали бы не только гликолиз, но и эти другие метаболические пути. Другое дело фруктозо-1,6-дифосфат – это настоящий промежуточный метаболит гликолиза. Тормозя его выработку, мы избирательно регулируем гликолиз. Краткое содержание урока
|




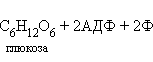 →
→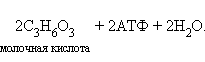
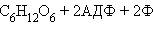 →
→