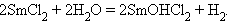Глава 8. Химические свойства элементов
8.4.1. Лантаноиды
Лантаноиды – это 14 элементов, следующих за лантаном, у которых к электронной конфигурации лантана последовательно добавляются 14 4f-электронов. В табл. 8.12 приведены электронные конфигурации лантаноидов и их наиболее устойчивые степени окисления. Общая электронная конфигурация лантаноидов – 4f2–145d0–16s2.
У церия на 4f-уровне находятся два электрона – один за счет увеличения порядкового номера по сравнению с лантаном на единицу, а другой переходит с 5d-уровня на 4f. До гадолиния происходит последовательное увеличение числа электронов на 4f-уровне, а уровень 5d остается незанятым. У гадолиния дополнительный электрон занимает 5d-уровень, давая электронную конфигурацию 4f75d16s2, а у следующего за гадолинием тербия происходит, аналогично церию, переход 5d-электрона на 4f-уровень (4f96s2). Далее до иттербия наблюдается монотонное увеличение числа электронов до 4f14, а у завершающего ряд лютеция вновь появляется 5d-электрон (4f145d16s2).
| Элемент |
Электронная конфигурация |
Степень окисления |
Элемент |
Электронная конфигурация |
Степень окисления |
| Церий |
Ce |
4f26s2 |
3, 4 |
Тербий |
Tb |
4f96s2 |
3, 4 |
| Празеодим |
Pr |
4f36s2 |
3, 4 |
Диспрозий |
Dy |
4f106s2 |
3, 4 |
| Неодим |
Nd |
4f46s2 |
3 |
Гольмий |
Ho |
4f116s2 |
3 |
| Прометий |
Pm |
4f56s2 |
3 |
Эрбий |
Er |
4f126s2 |
3 |
| Самарий |
Sm |
4f66s2 |
2, 3 |
Тулий |
Tm |
4f136s2 |
2, 3 |
| Европий |
Eu |
4f76s2 |
2, 3 |
Иттербий |
Yb |
4f146s2 |
2, 3 |
| Гадолиний |
Gd |
4f75d16s2 |
3 |
Лютеций |
Lu |
4f145d16s2 |
3 |
|
| Таблица 8.12 Электронные конфигурации и степени окисления 4f-элементов (лантаноидов)
|
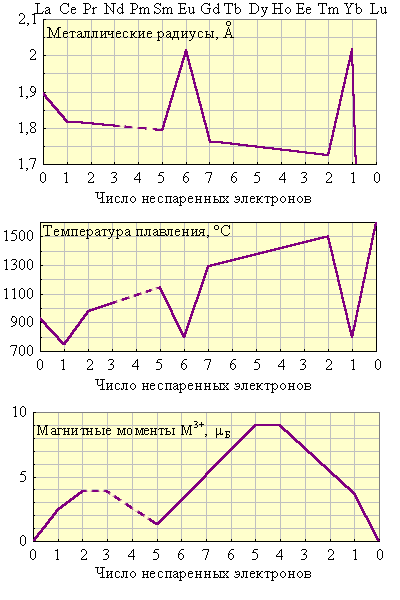
Периодический характер заполнения 4f-орбиталей сначала по одному, а потом по два электрона предопределяет внутреннюю периодичность свойств лантаноидов. Периодически изменяются металлические радиусы, степени окисления, температуры плавления и кипения, величины магнитных моментов, окраска и другие свойства (рис. 8.15). Участие 4f-электронов в образовании химической связи обусловлено предварительным возбуждением на уровень 5d. Энергия возбуждения одного электрона невелика, поэтому обычно лантаноиды проявляют степень окисления III (табл. 8.12, рис. 8.15). Однако некоторые из них проявляют так называемые аномальные степени окисления – 2, 4. Эти состояния окисления связывают с образованием наиболее устойчивых электронных конфигураций 4f0, 4f7, 4f14. Так, Ce и Tb приобретают конфигурации f0 и f7, переходя в состояние окисления +4, тогда как Eu и Yb имеют соответственно конфигурации – f7 и f14 в состоянии окисления +2. Однако существование Pr (IV), Sm (II), Dy (IV) и Tm (II) свидетельствует об относительности критерия особой устойчивости электронных конфигураций 4f0, 4f7 и 4f14. Как и для d-элементов, стабильность состояния окисления наряду с этим фактором характеризуется термодинамическими параметрами реального соединения.
Ограниченная возможность возбуждения 4f-электронов определяет сходство химических свойств лантаноидов в одинаковых степенях окисления. Основные изменения в свойствах лантаноидов являются следствием f-сжатия, то есть уменьшения эффективных радиусов атомов и ионов с увеличением порядкового номера.
В свободном состоянии лантаноиды – весьма активные металлы. В ряду напряжений они находятся значительно левее водорода (электродные потенциалы лантаноидов составляют около –2,4 В). Поэтому все лантаноиды взаимодействуют с водой с выделением водорода:
Соединения лантаноидов со степенью окисления IV проявляют окислительные свойства (Ce, Tb):
а соединения со степенью окисления II (Eu, Sm, Yb) – восстановительные, причем окисляются даже водой:
 1 1
|
| Рисунок 8.15 Вторичная периодичность металлических радиусов, температур плавления, степеней окисления, магнитных моментов и окраски лантаноидов
|
Лантаноиды очень реакционноспособны и легко взаимодействуют со многими элементами периодической системы: в кислороде сгорают при 200–400 °С с образованием Э2O3, а в атмосфере азота при 750–1000 °С образуют нитриды. Церий в порошкообразном состоянии легко воспламеняется на воздухе, поэтому его используют при изготовлении кремней для зажигалок. Лантаноиды взаимодействуют с галогенами, серой, углеродом, кремнием и фосфором. Химическая активность элементов в ряду Ce–Lu несколько уменьшается из-за уменьшения их радиусов. С водородом лантаноиды образуют солеобразные гидриды ЭH2 и ЭH3, которые по свойствам более близки к гидридам щелочно-земельных металлов, чем к гидридам d-элементов. С кислородом все лантаноиды образуют оксиды типа Э2O3, являющиеся химически и термически устойчивыми; так, La2O3 плавится при температуре 2000 °С, а CeO2 – около 2500 °С. Самарий, европий и иттербий, кроме оксидов Э2O3, образуют также монооксиды EuO, SmO, YbO. Церий легко образует оксид CeO2. Оксиды лантаноидов в воде нерастворимы, но энергично ее присоединяют с образованием гидроксидов:
Гидроксиды лантаноидов по силе уступают лишь гидроксидам щелочно-земельных металлов. Лантаноидное сжатие приводит к уменьшению ионности связи Э–ОН и уменьшению основности в ряду Ce(OH)3 – Lu(OH)3.
Лантаноиды используют в металлургии для легирования сталей, что повышает прочность, жаростойкость и коррозийную устойчивость последних. Такие стали применяют для изготовления деталей сверхзвуковых самолетов и оболочек искусственных спутников Земли.
Добавление оксида лантана в стекла повышает их показатель преломления (так называемая лантаноидная оптика). Радиационно-оптическую устойчивость стекол повышает CeO2. Стекла с неодимом используются в оптических квантовых генераторах. Оксиды гадолиния, самария и европия входят в состав защитных керамических покрытий от тепловых нейтронов в ядерных реакторах. Соединения лантаноидов используются в качестве катализаторов. Способность их соединяться с атмосферными газами используется для создания высокого вакуума.