

 |
 |
Многообразие органических реакций сводится к пяти типам: замещения, присоединения, отщепления, перегруппировки и окислительно-восстановительные.
В реакциях замещения водород или функциональная группа замещается на неводородный атом или другую функциональную группу:
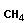 |
+ | 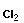 |
→ | 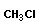 |
+ |  |
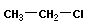 |
+ |  |
→ | 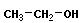 |
+ | 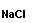 |
Реакции присоединения сопровождаются разрывом кратных связей:
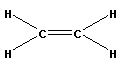 |
+ | 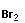 |
→ | 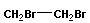 |
Реакции отщепления (элиминирования) приводят к образованию непредельных углеводородов:
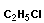 |
→ |  |
+ |  |
Реакции перегруппировки (изомеризации) приводят к образованию изомеров:
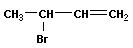 |
→ | 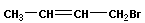 |
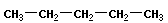 |
→ | 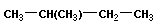 |
Реакции окисления и восстановления протекают с изменением степени окисления углеродного атома:
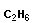 |
+ | 3,5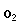 |
→ | 2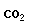 |
+ | 3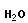 |
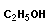 |
→ | 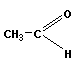 |
→ | 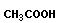 |
Все эти реакции протекают по двум механизмам, различающимся способом разрывания связей.
При свободнорадикальном механизме под действием излучения или температуры происходит гомологический разрыв связей (преимущественно малополярных) с образованием частиц, содержащих неспаренные электроны. Эти частицы – свободные радикалы – чрезвычайно реакционноспособны.
При ионном механизме происходит гетеролитический разрыв связей с образованием карбкатионов 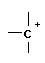 и карбанионов
и карбанионов 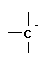 . Атакующий реагент, взаимодействующий с субстратом, может быть двух видов: нуклеофильным и электрофильным.
. Атакующий реагент, взаимодействующий с субстратом, может быть двух видов: нуклеофильным и электрофильным.
Нуклеофильные реагенты отдают электронную пару субстрату; электрофильные реагенты принимают электронную пару от субстрата. Карбкатионы обладают электрофильными свойствами, карбанионы – нуклеофильными.
Типичные нуклеофильные реагенты:
: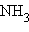 , :
, :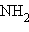 –R, :
–R, :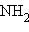 , :
, :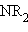 ,
, 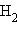 Ö, R–ÖH, R–Ö–R,
Ö, R–ÖH, R–Ö–R, 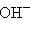 ,
, 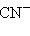 ,
, 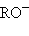 ,
, 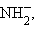 RCO
RCO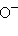 ,
, 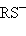 ,
, 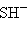 , Ha
, Ha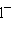 ,
, 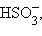 CN
CN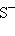 , CN
, CN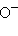 ,
, 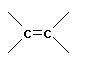 ,
, 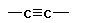 , Ph.
, Ph.
Типичные электрофильные реагенты:
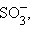
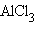 ,
, 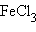 ,
, 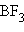 ,
, 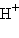 ,
, 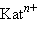 , R–Hal, альдегиды, кетоны, карбоновые кислоты, их галогенангидриды и сложные эфиры.
, R–Hal, альдегиды, кетоны, карбоновые кислоты, их галогенангидриды и сложные эфиры.
 |
 |
 |

